Cho phản ứng: 4P + 5O2 ⟶ 2P2O5
Quá trình oxi hóa là
Quá trình oxi hóa là quá trình chất khử nhường electron.
Vậy quá trình oxi hóa của phản ứng trên là
Cùng nhau thử sức với bài kiểm tra 15 phút Hóa 10 Chủ đề 4 Phản ứng Oxi hóa - khử.
Cho phản ứng: 4P + 5O2 ⟶ 2P2O5
Quá trình oxi hóa là
Quá trình oxi hóa là quá trình chất khử nhường electron.
Vậy quá trình oxi hóa của phản ứng trên là
Quá trình oxi hóa là
Quá trình oxi hóa (sự oxi hóa) là quá trình nhường electron.
Trong hợp chất SO3, số oxi hoá của sulfur (lưu huỳnh) là
Trong hợp chất SO3, số oxi hoá của sulfur (lưu huỳnh) là +6.
Hòa tan hoàn toàn 2,4 gam kim loại Mg vào dung dịch HNO3 loãng, giả sử chỉ thu được V lít khí N2 là sản phẩm khử duy nhất (đktc). Giá trị của V là :
nMg = 0,1 mol
Xét quá trình nhường và nhận electron của phản ứng
0,1 → 0,2
0,2 → 0,02
VN2 = 0,02.22,4 = 4,48 lít
Trong phân tử các hợp chất, thông thường số oxi hóa của oxygen là
Trong phân tử các hợp chất, thông thường số oxi hóa của oxygen là -2.
Số oxi hóa của đơn chất kim loại là:
Trong đơn chất, số oxi hóa của nguyên tử bằng 0.
⇒ Số oxi hóa của đơn chất kim loại là 0
Số oxi hóa của Na, Mg2+, Al3+ lần lượt là:
Dựa vào quy tắc xác định số oxi hóa, số oxi hóa của sodium, magnesium, aluminium trong Na, Mg2+, Al3+ lần lượt 0, +2, +3.
Cho sơ đồ phản ứng : Fe3O4 + HNO3 → Fe(NO3)3 + NO + H2O
Sau khi cân bằng, hệ số lần lượt của các chất là phương án nào sau đây?
Sự thay đổi số oxi hóa của các nguyên tử nguyên tố trước và sau phản ứng:
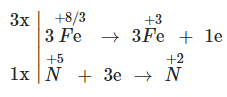
Cân bằng: 3Fe3O4 + 28HNO3 → 9Fe(NO3)3 + NO + 14H2O
Hệ số cân bằng của các phân tử là: 3, 28, 9, 1, 14
Trong phân tử oxygen, số oxi hóa của nguyên tử oxygen là
Phân tử O2 là đơn chất số oxi hóa của nguyên tử oxygen là 0.
Xác định tổng hệ số cân bằng tối giản của các chất trong phản ứng dưới đây:
K2Cr2O7 + HCl ⟶ Cl2 + KCl + CrCl3 + H2O
Sự thay đổi số oxi hóa của các nguyên tố:
Quá trình oxi hóa và quá trình khử:
Áp dụng nguyên tắc: tổng số electron nhường bằng tổng số electron nhận
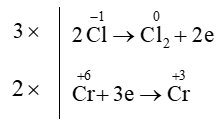
⇒ K2Cr2O7 + 14HCl ⟶ 3Cl2 + 2KCl + 2CrCl3 + 7H2O.
Vậy tổng hệ số cân bằng tối giản của các chất trong phản ứng là:
1 + 14 + 3 + 2 + 2 + 7 = 29
Số oxi hóa của nguyên tố N trong dãy các hợp chất nào dưới đây bằng nhau:
Trong NaNO3, HNO3, Fe(NO3)3; N2O5: số oxh của N là +5.
Trong ion đơn nguyên tử, số oxi hóa của nguyên tử bằng
Trong ion đơn nguyên tử, số oxi hóa của nguyên tử bằng điện tích ion.
Cho sơ đồ chuyển hóa của sulfur như sau:
S ![]() SO2
SO2 ![]() SO3
SO3 ![]() H2SO4
H2SO4 ![]() SO2
SO2
Mỗi mũi tên là một phản ứng hóa học. Có bao nhiêu phản ứng là phản ứng oxi hóa - khử?
Phản ứng oxi hóa - khử là phản ứng hóa học trong đó có sự thay đổi số oxi hóa của ít nhất một nguyên tố hóa học.
⇒ Các phản ứng oxi hóa khử là: S SO2; SO2
SO3; H2SO4
SO2.
Để một lượng bột iron ngoài không khí một thời gian thu được 5,68 gam hỗn hợp gồm Fe, FeO, Fe2O3 và Fe3O4. Hòa tan hoàn toàn hỗn hợp đó bằng dung dịch HNO3 loãng (dư), thu được 0,672 lít khí NO (sản phẩm khử duy nhất, ở đktc) và dung dịch chứa m gam muối Fe(NO3)3. Giá trị của m là bao nhiêu?
Quy đổi hỗn hợp oxide Fe thành Fe và O
Gọi x, y lần lượt là số mol của của Fe và O
nNO = 0,06 mol
Quá trình nhường e Fe0 → Fe+3 + 3e x → 3x | Quá trình nhận e O0 + 2e → O-2 x → 2y N+5 + 3e → N+2 0,09 ← 0,03 |
Áp dụng định luật bảo toàn e, ta có:
3x = 2y + 0,09 => 3x - 2y = 0,09 (1)
Mặt khác theo đề bài ta có: 56x + 16y = 5,68 (2)
Giải hệ phương trình (1), (2) ta được:
x = 0,08; y = 0,075
nFe(NO3)3 = nFe = 0,08 mol
=> mFe(NO3)3 = 19,36 gam.
Trong phản ứng oxi hóa - khử: 3CO + Fe2O3 → 2Fe + 3CO2. Chất khử là
Chất khử là Fe2O3
Hòa tan hoàn x mol CuFeS2 bằng dung dịch HNO3 đặc, nóng (dư) sinh ra y mol NO2 (sản phẩm khử duy nhất N+5). Biểu thức liên hệ giữa x và y là:
CuFeS2 → Cu+2 + Fe+3 + 2S+6 + 17e
x → 17x
N+5 + 1e → N+4
y ← y
Bảo toàn electron ta có:
Biểu thức liên hệ giữa x và y là y = 17x
Phản ứng oxi hóa – khử là
Phản ứng oxi hóa – khử là phản ứng hóa học trong đó có sự chuyển dịch electron giữa các chất phản ứng hay có sự thay đổi số oxi hóa của một số nguyên tử trong phân tử.
Trong phản ứng Fe + CuSO4 → FeSO4 + Cu thì một mol Fe đã
Trong phản ứng xảy ra quá trình:
mol: 1 → 2
⇒ Một mol Fe đã nhường 2 mol electron.
Cho các hợp chất sau: FeO; FeCl2; Fe(OH)3; Fe2O3; FeSO4. Số hợp chất trong đó sắt có số oxi hoá +2 là
Các hợp chất trong đó sắt có số oxi hoá +2 là: FeO; FeCl2; FeSO4.
Loại phản ứng nào sau đây luôn luôn không phải là phản ứng oxi hóa - khử.
Loại phản ứng luôn luôn không phải là phản ứng oxi hóa - khử là phản ứng trao đổi (vô cơ)
Ví dụ:
NaOH + HCl → NaCl + H2O
