Cách nào sau đây không làm tăng diện tích bề mặt của chất rắn?
Hòa tan chất rắn trong acid không làm tăng diện tích bề mặt của chất rắn.
Cùng nhau thử sức với bài kiểm tra 15 phút Hóa 10 Chương 6: Tốc độ phản ứng.
Cách nào sau đây không làm tăng diện tích bề mặt của chất rắn?
Hòa tan chất rắn trong acid không làm tăng diện tích bề mặt của chất rắn.
Yếu tố nào sau đây làm giảm tốc độ phản ứng
Thêm chất ức chế vào hỗn hợp chất tham gia làm giảm tốc độ của phản ứng.
Thực hiện 2 thí nghiệm theo hình vẽ sau:
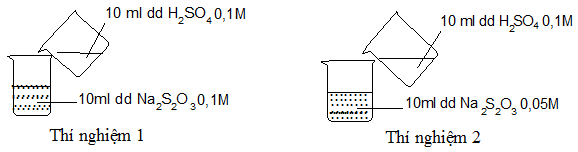
Phát biểu nào sau đây là đúng?
Sử dụng yếu tố nồng độ, thí nghiệm 1, nồng độ Na2S2O3 lớn hơn, tốc độ phản ứng xảy ra nhanh hơn Thí nghiệm 1 có kết tủa xuất hiện trước.
Tăng nhiệt độ của một hệ phản ứng sẽ dẫn đến sự va chạm có hiệu quả giữa các phân tử chất phản ứng. Tính chất của sự va chạm đó là:
Khi tăng nhiệt độ của một hệ phản ứng sẽ dẫn đến sự va chạm có hiệu quả giữa các phân tử chất phản ứng là tăng tốc.
độ phản ứng, nhưng khi đến một lúc nào đó, thì sự chạm có hiệu quả đó sẽ giảm dần do các chất đã kết hợp với nhau thành sản phẩm.
Cho các phát biểu sau về tốc độ phản ứng:
(a) Đơn vị tốc độ phản ứng là mol/ lít.
(b) Tốc độ phản ứng hoá học dùng để đánh giá mức độ xảy ra nhanh hay chậm của một phản ứng.
(c) Tốc độ trung bình của phản ứng là tốc độ phản ứng tại một thời điểm nào đó.
(d) Tốc độ tức thời của phản ứng là tốc độ được tính trong một khoảng thời gian phản ứng.
Số phát biểu sai là:
(a) Sai. Đơn vị của tốc độ phản ứng là: mol L-1s-1 (hay Ms-1),...
(b) Đúng.
(c) Sai. Tốc độ trung bình của phản ứng là tốc độ được tính trong một khoảng thời gian phản ứng.
(d) Sai. Tốc độ tức thời là tốc độ phản ứng tại một thời điểm nào đó.
Cho phản ứng hóa học sau:
Zn(s) + H2SO4(aq) → ZnSO4(aq) + H2(g)
Yếu tố nào sau đây không làm ảnh hưởng đến tốc độ phản ứng?
Thể tích dung dịch sulfuric acid không làm ảnh hưởng đến tốc độ phản ứng.
Khi nghiên cứu ảnh hưởng của nhiệt độ tới tốc độ của phản ứng giữa Zn(s) với HCl(aq), cho các mô tả sau đây:
(1) Khi đun nóng, bọt khí thoát ra nhanh hơn so với không đun nóng.
(2) Khi đun nóng, bọt khí thoát ra chậm hơn so với không đun nóng.
(3) Khi đun nóng, dây Zn tan nhanh hơn so với không đun nóng.
(4) Khi đun nóng, dây Zn tan chậm hơn so với không đun nóng.
Mô tả nào phản ánh đúng hiện tượng quan sát được khi làm thí nghiệm
Những mô tả phản ánh đúng hiện tượng quan sát được khi làm thí nghiệm:
(1) Khi đun nóng, bọt khí thoát ra nhanh hơn so với không đun nóng.
(3) Khi đun nóng, dây Zn tan nhanh hơn so với không đun nóng.
Cho phản ứng: X(g) + Y(g) → Z(g) + T(g)
Nếu tăng nồng độ chất Y lên 4 lần và nồng độ chất X giảm đi 2 lần thì tốc độ phản ứng tăng hay giảm bao nhiêu lần?
2X(g) + Y(g) → Z(g) + T(g)
Vban đầu = k.[X].[Y]2=kab2 (với a, b là nồng độ chất X, Y).
Vsau = k.
Vậy tốc độ tăng lên 8 lần
Cho phản ứng đơn giản xảy ra trong bình kín: 2CO(g) + O2(g) → 2CO2(g). Viết biểu thức tốc độ tức thời của phản ứng.
Biểu thức tốc độ tức thời của phản ứng:
Những ngày Tết, lượng thực phẩm nhiều được bảo quản trong tủ lạnh giúp cho thực phẩm được tươi lâu hơn, tốc độ phản ứng trên chịu ảnh hưởng của yếu tố nào?
Ảnh hưởng bởi yếu tố nhiệt độ. Quá trình bảo quản thực phẩm là hạn chế vi khuẩn hoạt động phá huỷ thức ăn, khi bảo quản trong tủ lạnh, nhiệt độ thấp sẽ giảm khả năng hoạt động của vi khuẩn, làm chậm quá trình phá huỷ thức ăn.
Một phản ứng có hệ số nhiệt độ Van’t Hoff bằng 3,5. Ở 20°C, tốc độ của phản ứng này bằng 0,2 Ms-1. Tốc độ của phản ứng ở 45°C là
Khi đốt than trong lòm, đậy nắp lò sẽ giữ than cháy được lâu hơn. Yếu tố ảnh hưởng đến tốc độ phản ứng được vận dụng trong ví dụ trên là
Đậy nắp lò sẽ làm giảm nồng độ oxygen tham gia phản ứng đốt cháy than, do đó tốc độ phản ứng giảm nên than cháy được lâu hơn.
Khi tăng nồng độ chất tham gia, thì
Khi tăng nồng độ chất tham gia, thì tốc độ phản ứng tăng.
Cho phản ứng: 2KClO3(s) ![]() 2KCl(s) + 3O2(g). Yếu tố không ảnh hưởng đến tốc độ của phản ứng trên là:
2KCl(s) + 3O2(g). Yếu tố không ảnh hưởng đến tốc độ của phản ứng trên là:
Áp suất không ảnh hưởng đến phản ứng trên do phản ứng không có chất khí tham gia.
Dùng bình chứa oxygen thay cho dùng không khí để đốt cháy acetylene. Yếu tố ảnh hưởng đến tốc độ của quá trình biến đổi này là
Nồng độ khí oxygen trong bình chứa oxygen cao hơn nhiều so với ngoài không khí Tốc độ phản ứng tăng.
Phát biểu nào sau đây đúng:
Khi đốt củi, nếu thêm 1 ít dầu hỏa lửa sẽ cháy to hơn, nhưng dầu hỏa không phải chất xúc tác. Vì chất xúc tác không bị hao hụt trong quá trình phản ứng.
Trong quá trình làm sữa chua lúc đầu người ta phải pha sữa trong nước ấm và thêm men là để tăng tốc độ quá trình gây chua, sau đó bảo quản ở nhiệt độ thấp để kìm hãm tốc độ phản ứng của quá trình này.
Dùng quạt thông gió trong bễ lò rèn là vận dụng yếu tố nồng độ, ở đây là nồng độ oxygen
Cho phản ứng 3O2 → 2O3. Nồng độ oxygen sau 5s đầu là 0,015 mol/L. Sau 15s tiếp thì nồng độ của oxygen là 0,01 mol/L. Tốc độ phản ứng trên tính theo oxygen là:
Tốc độ phản ứng trung bình:
Công thức liên hệ giữa hệ số Van’t Hoff với tốc độ phản ứng và nhiệt độ là
Mối liên hệ của hệ số Van’t Hoff với tốc độ và nhiệt độ như sau:
=
Trong đó v2, v1 là tốc độ phản ứng ở nhiệt độ T2 và T1 tương ứng.
Trong các phản ứng hóa học sau, phản ứng nào xảy ra nhanh?
Áp suất không ảnh hưởng đến tốc độ phản ứng nào sau đây?
Phản ứng 2KI (aq) + H2O2 (aq) → I2 (s) + 2KOH (aq)
Thay đổi áp suất không làm ảnh hưởng đến tốc độ của phản ứng vì không có sự tham gia của chất khí.
