Cl2 có thể oxi hóa được Br- thành Br2 tính oxi hóa của Cl2 mạnh hơn Br2.
Halogen nào sau đây dùng để khử trùng nước sinh hoạt?
Halogen được dùng để khử trùng nước sinh hoạt là Cl2.
Khoahoc.vn xin gửi tới bạn đọc Đề thi cuối học kì 2 môn Hóa 10, cùng nhau luyện tập và xem kết quả nha!
Halogen nào sau đây dùng để khử trùng nước sinh hoạt?
Halogen được dùng để khử trùng nước sinh hoạt là Cl2.
Cho các dung dịch sau: NaCl, KI, Mg(NO3)2, AgNO3. Chỉ dùng thuốc thử duy nhất là dung dịch HCl thì nhận biết được bao nhiêu dung dịch trên?
Dấu hiệu nhận biết:
| Thuốc thử/chất | NaCl | KI | Mg(NO3)2 | AgNO3 |
| HCl | Không phản ứng | Không phản ứng | Không phản ứng | Kết tủa trắng |
| AgNO3 | Kết tủa trắng | Kết tủa vàng đậm | Không phản ứng |
Phương trình hóa học:
AgNO3 + NaCl → AgCl↓ + NaNO3
AgNO3 + KI → AgI↓ + KNO3
Những hydrogen halide có thể thu được khi cho H2SO4 đặc lần lượt tác dụng với các muối NaF, NaCl, NaBr, NaI là:
Hydrogen halide có thể là HF và HCl.
Không thể là HBr và HI vì khí HBr và HI sinh ra phản ứng được với H2SO4 đặc nóng.
Cho các phản ứng hóa học sau, phản ứng nào chứng minh Cl2 có tính oxi hoá mạnh hơn Br2?
Cl2 có thể oxi hóa được Br- thành Br2 tính oxi hóa của Cl2 mạnh hơn Br2.
Một nhà máy nước sử dụng 5 mg Cl2 để khử trùng 1 lít nước sinh hoạt. Khối lượng Cl2 nhà máy cần dùng để khử trùng 100 m3 nước sinh hoạt?
100 m3 = 100 000 dm3 = 100 000 lít
Khử trùng 1 lít nước sinh hoạt cần 5 mg Cl2
Khử trùng 100 000 lít nước sinh hoạt cần 5.100 000 = 500 000 mg Cl2 = 500 g Cl2
Dung dịch HF được dùng để khắc chữ vẽ hình lên thủy tinh nhờ phản ứng với chất nào sau đây?
Acid hydrofloric acid có khả năng hoàn tan silicon dioxide nên được sử dụng để khắc các chi tiết lên thủy tinh theo phản ứng:
HF + SiO2 → SiF4 + 2H2O
Nguyên tử khối trung bình của chlorine là 35,5. Chlorine trong tự nhiên có 2 đồng vị là 35Cl và 37Cl. Phần trăm về khối lượng của ![]() chứa trong HClO4 (với hydrogen là đồng vị
chứa trong HClO4 (với hydrogen là đồng vị ![]() , oxygen là đồng vị
, oxygen là đồng vị ![]() ) là giá trị nào sau đây?
) là giá trị nào sau đây?
Gọi phần trăm đồng vị 35Cl = x ⇒ phần trăm đồng vị 37Cl = 100 – x.
Ta có:
⇒ x = 75%
⇒ Phần trăm đồng vị 37Cl = 25%
Phần trăm khối lượng của 37Cl trong HClO4 là:
Đốt cháy 29,25 gam zinc trong khí chlorine thu được 48,96 gam zinc chloride (ZnCl2). Hiệu suất của phản ứng trên là:
nZn = 0,45 (mol); nZnCl2 = 0,36 (mol)
Phương trình hóa học:
Zn + Cl2 ZnCl2
mol: 0,36 0,36
Quy ước về dấu của nhiệt phản ứng (![]() ) nào sau đây là đúng?
) nào sau đây là đúng?
Quy ước về dấu của nhiệt phản ứng :
- Phản ứng tỏa nhiệt có < 0.
- Phản ứng thu nhiệt có > 0.
Cho m gam hỗn hợp tinh thể gồm NaBr tác dụng vừa đủ với H2SO4 đặc ở điều kiện thích hợp thu được hỗn hợp khí X ở điều kiện thường. Ở điều kiện thích hợp X tác dụng vừa đủ với nhau tạo thành 9,6 gam chất rắn màu vàng và một chất lỏng không làm đổi màu quỳ tím. Giá trị của m là:
Phương trình hóa học:
2NaBr + H2SO4 Na2SO4 + Br2 + SO2 + 2H2O
8NaI + 5H2SO4 4Na2SO4 + 4I2 + H2S + 4H2O
2H2S + SO2 → 3S + 2H2O
mol: 0,2 ← 0,1 ← 0,3
Chất rắn màu vàng là lưu huỳnh, nS = 0,3 mol
Theo phương trình hóa học ta có:
nNaI = 8.nH2S = 1,6 mol
nNaBr = 2nSO2 = 0,2 mol
⇒ m = mNaI + mNaBr = 260,6 gam
Thực chất đây là phản ứng oxi hóa I- và Br-.
Cho 2 mẫu BaSO3 có khối lượng bằng nhau và 2 cốc chứa 50 ml dung dịch HCl 0,1 M như hình sau. Hỏi ở cốc nào mẫu BaSO3 tan nhanh hơn?
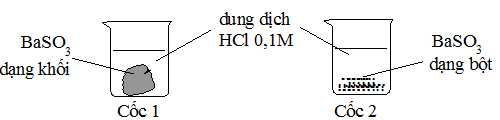
Sử dụng yếu tố diện tích tiếp xúc, thí nghiệm 2 BaSO3 dạng bột sẽ làm tăng diện tích tiếp xúc, tốc độ phản ứng xảy ra nhanh hơn.
Phản ứng phân huỷ ethyl iodide trong pha khí xảy ra như sau:
C2H5I → C2H4 + HI
Ở 127°C, hằng số tốc độ của phản ứng là 1,60.10−7 s−1; ở 227°C là 4,25.10−4 s−1. Tính hệ số nhiệt độ của phản ứng trên.
Hằng số tốc độ tỉ lệ thuận với tốc độ phản ứng.
Gọi hệ số nhiệt độ là γ, ta có:
⇒ γ10 = 2656,25 ⇒ γ = 2,2.
Tính số phát biểu không đúng trong các phát biểu sau:
(a) Chất khử (chất bị oxi hoá) là chất nhường electron và chất oxi hoá (chất bị khử) là chất nhận electron.
(b) Quá trình nhường electron là quá trình khử và quá trình nhận electron là quá trình oxi hoá.
(c) Trong quá trình oxi hoá, chất oxi hoá bị oxi hoá lên số oxi hoá cao hơn.
(d) Trong quá trình khử, chất khử bị khử xuống số oxi hoá thấp hơn.
(e) Phản ứng trong đó có sự trao đổi electron là phản ứng oxi hoá - khử.
Phát biểu (b) sai vì: Quá trình nhường electron là quá trình oxi hóa và quá trình nhận electron là quá trình khử.
Phát biểu (c) sai vì: Trong quá trình oxi hoá, chất khử bị oxi hoá lên số oxi hoá cao hơn.
Phát biểu (d) sai vì: Trong quá trình khử, chất oxi hóa bị khử xuống số oxi hoá thấp hơn.
Cho phản ứng hóa học sau:
Mg (s) + 2HCl (aq) → MgCl2 (aq) + H2 (g)
Sau 40 giây, nồng độ của dung dịch HCl giảm tử 0,6 M về còn 0,4 M. Tốc độ trung bình của phản ứng theo nồng độ của HCl trong 40 giây là
Tốc độ trung bình của phản ứng theo HCl trong 40 giây là:
Cho phản ứng tạo thành propene từ propyne:
CH3–C≡CH(g) + H2(g) ![]() CH3–CH=CH2(g)
CH3–CH=CH2(g)
Cho giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn:
| Liên kết | C–H | C–C | C=C | C≡C | H–H |
| Eb (kJ/mol) | 413 | 347 | 614 | 839 | 432 |
Biến thiên enthalpy chuẩn của phản ứng là
= Eb(C≡C) + Eb(C−C) + 4.Eb(C−H) + Eb(H−H) − Eb(C=C) − Eb(C−C) − 6.Eb(C−H)
= Eb(C≡C) – Eb(C=C) + Eb(H–H) – 2Eb(C–H)
= 839 – 614 + 432 – 2.413
= –169 kJ.
Halogen không có tính khử là
Fluorine chỉ có tính oxi hóa, không có tính khử.
Trong các chất sau đây, chất nào dùng để nhận biết hồ tinh bột?
Chỉ thị thường dùng để nhận biết dung dịch I2 là hồ tinh bột.
Hiện tượng: Dung dịch chuyển màu xanh tím.
Cho 4 đơn chất F2, Cl2, Br2, I2. Chất có nhiệt độ sôi cao nhất là
Nhiệt độ nóng chảy, nhiệt độ sôi tăng từ I2 đến F2.
Quy tắc xác định số oxi hoá nào sau đây là không đúng?
Trong hợp chất, số oxi hoá của kim loại kiềm thổ là +2.
Tại sao nhiều phản ứng hóa học trong công nghiệp cần tiến hành ở nhiệt độ cao và sử dụng chất xúc tác?
Do trong công nghiệp cần sản xuất các chất với một lượng lớn, thời gian sản xuất nhanh để đạt hiệu quả kinh tế nên nên cần tốc độ phản ứng nhanh.
Ở nhiệt độ thường, tốc độ các phản ứng xảy ra chậm nên cần thêm xúc tác và tăng nhiệt độ để tốc độ phản ứng xảy ra nhanh hơn.
Enzyme catalase phân huỷ hydrogen peroxide thành oxygen và nước nhanh gấp khoảng 107 lần sự phân huỷ khi không có xúc tác. Giả sử một phản ứng không có xúc tác phân huỷ một lượng hydrogen peroxide mất 360 ngày, hãy tính thời gian (theo giây) cho sự phân huỷ cùng một lượng hydrogen peroxide đó khi sử dụng enzyme catalase làm xúc tác.
Thời gian phân hủy (theo giây) khi phân huỷ cùng một lượng hydrogen peroxide đó, sử dụng enzyme catalase làm xúc tác là:
Để hạn chế sự ôi thiu thực phẩm do các phản ứng của oxygen cũng như sự hoạt động của vi khuẩn, người ta thường bơm khí nào sau đây vào các túi đựng thực phẩm trước khi đóng gói?
Thực phẩm bị ôi thiu do các phản ứng oxi hóa của oxygen cũng như hoạt động của vi khuẩn. Để hạn chế sự ôi thiu, người ta bơm khí N2 hoặc CO2 vào túi đựng thực phẩm trước khi đóng gói. Khi đó nồng độ khí oxygen sau khi bơm N2 hoặc CO2 chỉ còn 2 – 5%.
Cho 8,4 gam Fe phản ứng hoàn toàn với lượng dư dung dịch HNO3, thể tích khí NO (đkc) thu được là (coi NO là sản phẩm khử duy nhất)
nFe = 0,15 (mol)
Gọi số mol NO là a (mol), ta có các quá trình:
0,15 → 0,45 mol
3a ← a mol
⇒ 3a = 0,45 ⇔ a = 0,15
VNO = 0,15.24,79 = 3,7185 (L).
Cho phản ứng xảy ra ở điều kiện chuẩn sau: 2NO2(g) → N2O4(g). Biết NO2 và N2O4 có ![]() tương ứng lần lượt là 33,18 kJ/mol và 9,16 kJ/mol. Phản ứng
tương ứng lần lượt là 33,18 kJ/mol và 9,16 kJ/mol. Phản ứng
=
(N2O4) – 2.
(NO2) = 9,16 – 2,33,18 = –57,2 (kJ) < 0
⇒ Phản ứng toả nhiệt, N2O4 bền vững hơn NO2.
Cho phản ứng: 2KClO3(s) ![]() 2KCl(s) + 3O2(g). Yếu tố không ảnh hưởng đến tốc độ của phản ứng trên là:
2KCl(s) + 3O2(g). Yếu tố không ảnh hưởng đến tốc độ của phản ứng trên là:
Áp suất không ảnh hưởng đến phản ứng trên do phản ứng không có chất khí tham gia.
Phương trình hóa học nào sau đây viết sai?
Phương trình hóa học viết sai là: Cl2 + Fe → FeCl2.
Sửa lại: 3Cl2 + 2Fe → 2FeCl3.
Phát biểu nào sau đây không đúng?
Nhiệt độ vùng cao thấp hơn nhiệt độ ở vùng thấp → Nhiên liệu ở vùng cao cháy chậm hơn.
Trong những phản ứng hoá học xảy ra theo các phương trình dưới đây, những phản ứng nào là phản ứng oxi hoá - khử?
(1) PCl3 + Cl2 → PCl5
(2) Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
(3) CO2 + 2LiOH → Li2CO3 + H2O
(4) FeCl2 + 2NaOH → Fe(OH)2 + 2NaCl
Chọn phương án đúng.
Phản ứng (1) và (2) là phản ứng oxi hóa – khử do có sự thay đổi số oxi hóa của một số nguyên tố trong phản ứng.
Số oxi hoá của carbon và oxygen trong C2O42- lần lượt là:
Ta có số oxi hóa của oxygen trong C2O42– là –2:
Gọi số oxi hóa của C là x thì:
2.x + 4.(–2) = –2 ⇒ x = +3.
Phát biểu nào dưới đây là sai?
C sai, vì không phải tất cả các phản ứng mà chất tham gia có chứa nguyên tố oxygen đều toả nhiệt.
Ví dụ: CaCO3 → CaO + CO2 là phản ứng thu nhiệt.
Phương trình nhiệt hóa học nào sau đây ứng với sơ đồ biểu diễn biến thiên enthalpy của phản ứng sau?
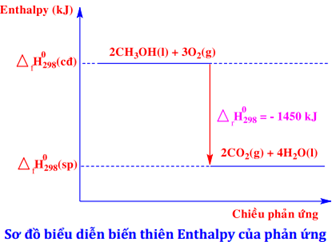
Quan sát sơ đồ ta có phương trình nhiệt hoá học ứng với sơ đồ biểu diễn biến thiên enthalpy của phản ứng là:
2CH3OH(l) + 3O2(g) → 2CO2(g) + 4H2O(l). = –1450 kJ.
Cho các phản ứng sau:
(1) A + HCl → MnCl2 + B↑ + H2O.
(2) B + C → nước Javel.
(3) C + HCl → D + H2O.
(4) D + H2O ![]() C + B↑+ E↑.
C + B↑+ E↑.
Chất Khí E là chất nào sau đây?
(1) MnO2 + HCl → MnCl2 + Cl2 (B) + H2O.
(2) Cl2 + 2NaOH (C) → NaCl + NaClO + H2O.
(3) NaOH + HCl → NaCl (D) + H2O.
(4) 2NaCl + 2H2O 2NaOH + Cl2 + H2 (E).
Khí H2 có thể được điều chế bằng cách cho miếng sắt vào dung dịch HCl. Một học sinh đề xuất các biện pháp sau đây để làm tăng tốc độ điều chế khí H2 từ cách này:
(1) Tăng nồng độ dung dịch HCl.
(2) Dùng sắt bột và khuấy nhẹ trong quá trình phản ứng..
(3) Tăng áp suất của hệ phản ứng.
(4) Đun nóng ống nghiệm chứa hỗn hợp Fe và HCl.
Số biện pháp hiệu quả là
Phản ứng xảy ra:
Fe + HCl FeCl2 + H2
Các biện pháp hiệu quả để tăng tốc độ phản ứng là: (1); (2); (4).
Phản ứng không có chất khí tham gia nên tăng áp suất của hệ phản ứng không làm tăng tốc độ phản ứng.
Cho m gam một đơn chất halogen (X2) tác dụng hết với magnesium thì thu được 9,5 gam muối. Mặt khác cho m gam X2 tác dụng hết với aluminium thì thu được 8,9 gam muối. Đơn chất halogen X2 là
Phương trình hóa học:
Mg + X2 → MgX2
2Al + 3X2 → 2AlX3
Bảo toàn nguyên tố X:
2nMgX2 = 3nAlX3
X = 35,5 (Cl)
Tính khử của các hydrohalic acid HX được sắp xếp giảm dần theo thứ tự:
Theo chiều HF HCl
HBr
HI
Tính acid tăng dần, tính khử tăng dần.
Thứ tự giảm dần tính khử: HI > HBr > HCl > HF.
Phản ứng trong đó HCl thể hiện tính khử là
Ta có:
Nguyên tử Cl trong phân tử HCl nhường electron HCl thể hiện tính khử.
Chlorine có thể phản ứng được với tất cả các chất trong dãy nào sau đây?
Chlorine không phản ứng được với oxide kim loại Loại phương án có CuO, ZnO
Chlorine không phản ứng trực tiếp với oxygen.
Chlorine có thể phản ứng được với NaBr, NaI, NaOH.
Ở 10∘C hai phản ứng xảy ra với cùng một tốc độ (v1 = v2). Hệ số nhiệt độ của phản ứng thứ nhất và thứ hai là 2 và 3. Nếu ở phản ứng thứ nhất nhiệt độ tăng lên 50∘C và phản ứng thứ hai nhiệt độ tăng lên 30∘C thì tốc độ phản ứng trên có tỉ lệ như thế nào?
Gọi tốc độ của phản ứng thứ nhất sau khi tăng lên 50oC là v1'.
Gọi tốc độ của phản ứng thứ hait sau khi tăng lên 30oC là v2'.
Ta có:
Tỉ lệ của tốc độ của hai phản ứng sau khi tăng nhiệt độ là:
Trong nhóm halogen, sự biến đổi tính chất nào sau đây của đơn chất đi từ fluorine đến iodine là đúng?
Thể của các halogen ở điều kiện thường biến đổi từ khí (fluorine, chlorine) đến lỏng (bromine) và rắn (iodine), phù hợp với xu hướng tăng khối lượng phân tử và sự tương tác giữa các phân tử.
Có hỗn hợp gồm hai muối NaCl và NaBr. Khi cho dung dịch AgNO3 vừa đủ vào hỗn hợp trên người ta thu được lượng kết tủa bằng khối lượng AgNO3 tham gia phản ứng. Tìm thành phần phần trăm khối lượng NaBr trong hỗn hợp ban đầu.
Gọi số mol của NaCl và NaBr lần lượt là a, b:
NaCl + AgNO3 → AgCl + NaNO3
a a a
NaBr + AgNO3 → AgBr + NaNO3
b b b
170a – 143,5a = 188b – 170b
Theo bài ra ta có lượng kết tủa bằng khối lượng AgNO3 tham gia phản ứng nên:
26,5a = 18b
%NaBr = 100% - 27,84% = 72,16%
