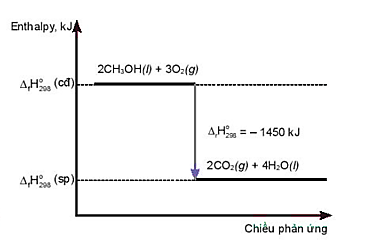
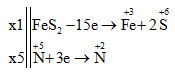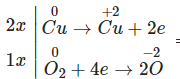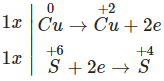Chất nào sau đây trong các phản ứng chỉ đóng vai trò là chất khử trong các phản ứng?
Trong hợp chất, K chỉ có số oxi hóa +1. Do đó khi tham gia phản ứng hóa học, K chỉ đóng vai trò là chất khử.
Chú ý: Trong hợp chất, H ngoài số oxi hóa +1, còn có số oxi hóa -1 (trong H2O2,...)