Tổng số các hạt proton, neutron và electron trong nguyên tử của một nguyên tố là 40. Biết số hạt neutron lớn hơn số hạt proton là 1. Cho biết nguyên tố trên thuộc loại nguyên tố nào?
Gọi số hiệu nguyên tử, số neutron của nguyên tố trên lần lượt là Z, N.
Ta có hệ phương trình:
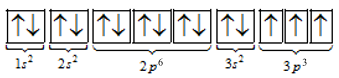
Cấu hình electron của nguyên tố là: 1s22s22p63s23p1
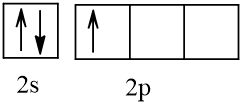
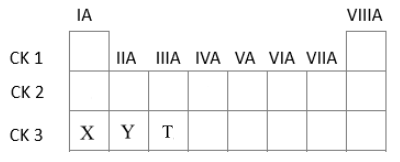
Nhận thấy electron cuối cùng điền vào phân lớp p nguyên tố trên thuộc loại nguyên tố p.