Quy tắc octet
I. Quy tắc octet
Quy tắc octet lần đầu được đưa ra bởi Lewis (nhà hóa học, vật lí người Mỹ) để lí giải xu hướng các nguyên tử trở nên bền vững hơn trong phản ứng hóa học.
Quy tắc octet: Trong phản ứng hóa học, các nguyên tử có xu hướng hình thành lớp vỏ bền vững như của khí hiếm.
Các nguyên tử khí hiếm có lớp electron ngoài cùng đã bão hoà với 8 electron (trừ helium có 2 electron lớp ngoài cùng) nên rất khó tham gia vào các phản ứng hoá học.
Các nguyên tử liên kết với nhau theo xu hướng chung là tạo ra lớp electron ngoài cùng như của khí hiếm gần nhất để mỗi nguyên tử trở nên bền vững hơn.
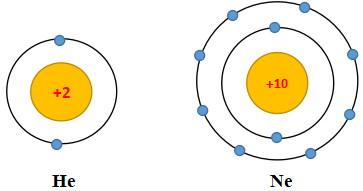
Mô hình cấu tạo nguyên tử của He và Ne
Các nguyên tử liên kết với nhau theo xu hướng chung là tạo ra lớp electron ngoài cùng như của khí hiếm gần nhất để mỗi nguyên tử đó trở nên bền vững hơn.
II. Vận dụng quy tắc octet trong quá trình hình thành liên kết hóa học của các nguyên tố nhóm A
Trong quá trình hình thành liên kết hóa học, các nguyên tử có xu hướng nhường, nhận hoặc góp chung electron để đạt được cấu hình electron bền vững như của khí hiếm gần nhất với 8 electron ở lớp ngoài cùng (hoặc có 2 electron ở lớp ngoài cùng như của He).
Ví dụ 1: O (Z = 8) có cấu hình electron là 1s22s22p4
Oxygen có 6 electron lớp ngoài cùng. Vậy xu hướng cơ bản của nguyên tử oxygen khi hình thành liên kết hóa học là nhận thêm 2 electron để đạt được lớp vỏ có 8 electron ở lớp ngoài cùng như của khí hiếm Ar.
Sơ đồ nguyên tử O nhận thêm 2 electron vào lớp ngoài cùng:

Sơ đồ nguyên tử oxygen nhận thêm 2 electron vào lớp ngoài cùng
Ví dụ 2: K (Z = 19) có cấu hình electron là: 1s22s22p63s23p64s1. Vậy K có 1 electron lớp vỏ ngoài cùng. Nguyên tử K có xu hướng nhường đi 1 electron để trở thành ion mang điện tích dương, kí hiệu là K+.
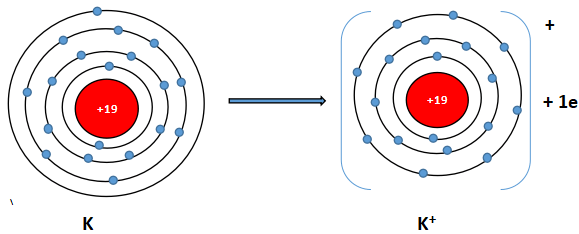 Sơ đồ nguyên tử potassium nhường đi 1 electron vào lớp ngoài cùng
Sơ đồ nguyên tử potassium nhường đi 1 electron vào lớp ngoài cùng
Ví dụ 3: Nguyên tử N (Z = 7) có cấu hình electron là 1s22s22p3
Nguyên tử H (Z = 1) có cấu hình electron là 1s1
Để đạt được cấu hình của khí hiếm gần nhất, nguyên tử N cần thêm 3 electron, nguyên tử H cần thêm 1 electron. Vì vậy mỗi nguyên tử H sẽ góp chung 1 electron với nguyên tử N để tạo thành 3 cặp electron chung.
Các cặp electron chung cho phân tử NH3
 Sơ đồ góp chung electron của các nguyên tử trong phân tử NH3
Sơ đồ góp chung electron của các nguyên tử trong phân tử NH3
Nhận xét:
- Các kim loại có 1, 2 hoặc 3 electron ở lớp ngoài cùng có xu hướng nhường bớt toàn bộ các electron này để tạo thành ion dương tương ứng có 8 electron ở lớp ngoài cùng.
- Trong cùng chu kì, nguyên tử có 1 electron ở lớp ngoài cùng (các kim loại kiềm) dễ nhường electron hơn nên có tính kim loại mạnh nhất.
- Ngoài cách các nguyên tử nhường và nhận electron để hình thành liên kết ion, quy tắc octet có thể đạt được bằng cách góp chung electron.
Lưu ý: Quy tắc octet có một số ngoại lệ như: SF6 (lớp vỏ ngoài cùng của S có 12 electron); PCl5 (lớp vỏ ngoài cùng của S có 10 electron), ...
Nội dung cùng chủ đề
-
Chủ đề 1. Cấu tạo nguyên tử
-
Chủ đề 2. Bảng tuần hoàn các nguyên tố hóa học
-
Đề thi giữa học kì 1
-
Chủ đề 3. Liên kết hóa học
-
Đề thi cuối học kì 1
-
Chủ đề 4. Phản ứng Oxi hóa - khử
-
Chủ đề 5. Năng lượng hóa học
-
Đề thi giữa học kì 2
-
Chủ đề 6. Tốc độ phản ứng hóa học
-
Chủ đề 7. Nguyên tố nhóm VIIA (Nhóm Halogen)
-
Đề thi cuối học kì 2







